Extras din curs
5 Arhitectura spatiala a cristalelor
3.1.- Starea fizică a materialelor
Toate substanţele pot fi, în principiu, în trei stări fizice distincte: solide, lichide sau gazoase, practic fiind posibilă şi o a patra stare şi anume cea de plasmă Fiecare stare există ca o consecinţă a bilanţului dintre energia de coeziune (de apropiere dintre atomi) şi energia termică (tendinţa de separare).
Energia termică Et care este rezultatul mişcării continui a atomilor este proporţională cu temperatura absolută T:
Et = kT (2.46)
unde : k = 1,38 10-23 J.K-1 este constanta lui Boltzman ( k = R/NA, R - constanta gazelor perfecte, iar NA - numărul lui Avogadro). Energia de coeziune este energia necesară pentru a desface sistemul în elementele sale constitutive, cum s-ar spune, pentru vaporizarea substanţei. Ea este mult mai mare pentru corpurile a căror elemente constitutive sunt legate prin legături puternice ( metale, ceramice) şi destul de mică în cazul în care moleculele (F2, Cl2, , moleculele organice) sau atomii (gaze rare) sunt legaţi prin forţe de legătură slabe. Energia termică este proporţională cu temperatura, în timp ce energia de coeziune, în primă aproximaţie, este independentă. Aceasta explică tranziţia structurilor şi stărilor substanţelor cu temperatura. In fig. 2.15 este prezentată această evoluţie. Atunci când energia termică este mai mare decât energia de coeziune (situaţie specifică temperaturilor înalte), toate stările ce implică ordonarea atomilor sunt excluse.
Grafic cele tri stări fizice ale unei substanţe sunt prezentate în fig.1.
Fig.2.15.- Schiţa evoluţiei gradului de organizare a atomilor cu creşterea temperaturii
Trecerea de la o stare la alta este ilustrată în fig. , schimbarea de stare fiind determinată de creşterea energiei sistemului.
Fig. Procesele fizice şi transformările de stare ale materiei
Trecerea de la o stare fizică la alta în funcţie de parametrii energetici (temperatură, presiune) este ilustrată în diagrama de stare din fig.
Fig. - Diagrama de faze a unei substanţe pure
O comparaţie a comportării macroscopice a stărilor fizice ale materiei este dată în tab. , iar la nivel nanoscopic comparaţia este prezentată în tab.
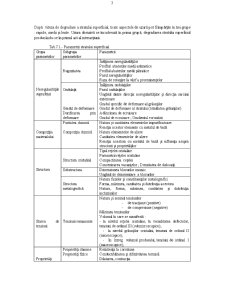
Tab. – Comparaţie între principalele caracteristici ale stărilor fizice ale materiei.
Comportarea macroscopică
Faza Păstrează volumul Păstrează forma Compresibile Viteza de curgere Viteza de difuzie
Solide
Cristaline
Da Da Nu Mică
Mare Mică
Mare
Cristale
Lichide
Da Nu Nu
Lichide
Da Nu Nu
Gaze
Nu Nu Da
Tab. Comportarea nanoscopică a stărilor fizice ale materiei
Comportarea nanoscopică
Faza Gradul de
orientare Ordinea de
translaţie Forţa
intermoleculară Distanţa
interatomică
sau
intermoleculară
Solide cristaline Ordine depărtată
Da
Puternică
Slabă Mică
Mare
Cristale lichide Ordine depărtată
Nu
Lichide
Ordine
apropiată Nu
Gaze
Dezordine
totală Nu
3.1.1.- Dezordine completă : gaze
Gazele ocupă tot volumul pus la dispoziţia lor, sunt compresibile, iar fiecare dintre particulele care le compun este în mişcare continuă din cauza agitaţiei termice. Intr-un gaz numărul de particule pe unitatea de volum este în funcţie de presiune şi de temperatură., iar între ele nu se poate defini o relaţie de ordine, poziţia unei particule în raport cu alta fiind arbitrară, modificându-se continuu în timp.
Taoate gazele se pot amesteca în orice proporţie. O fază gazoasă poate avea mai mulţi constituenţi : ex.: aerul (N2, O2, H2O ). Forţele de legătură intermoleculare sunt slabe şi ca urmare, gazeele nu-şi pot păstra forma şi nici volumul.
3.1.2.- Lichide şi solide amorfe
Unele lichide sunt miscibile între ele, ex. apă + alcool (formând o singură fază), altele sunt nemiscibile, ex. apă + ulei (prin separare formează două faze). Forţele interatomice sau intermoleculare sunt mai puternice decât în cazul gazelor dar mai slabe decât cele specifice solidelor. Proprietatea de bază a lichidelor este vâscozitatea care reprezintă rezistenţa la curgere a acestora Vâscozitatea este puternic influenţată de temperatură întrucât este dependentă de forţele de atracţie dintre molecule.
Ca şi la solide, volumul ocupat de un lichid este constant şi în primă aproximaţie, independent de presiune (atomii de pe o anumită direcţie sunt în contact unii cu alţii). Intr-un lichid, diametrul mediu al unui atom este comparabil cu cel al unui atom dintr-un solid, respectiv de 0,25 nm. Spre deosebire de solide, în lichide, din cauza agitaţiei termice, atomii sau grupurile de atomi sunt în mişcare continuă, modificându-şi rapid poziţia
Ordinea apropiată conferă lichidelor şi solidelor amorfe izotropie, proprietăţile fiind aceleaşi în orice direcţie în care sunt măsurate. In sfârşit, dacă baza de măsură este suficient de mare - o sută de distanţe interatomice - densitatea atomilor pe unitatea de lungime este aceeaşi în toate direcţiile. Un lichid este incompresibil deoarece atomii pe o direcţie sunt în contact. Din cauza agitaţiei termice şi mişcării atomilor, o astfel de structură prezintă o slabă rezistenţă la forfecare şi o slabă rezistenţă la curgere. Rezistenţa la forfecare este măsurată prin vâscozitate.
Dacă un lichid pur (metal sau apă) este răcit sub temperatura de topire, el se solidifică. Trecerea de la starea lichidă la cea solidă cristalină se face direct fără o creştere notabilă a vâscozităţii lichidului. Solidificarea se produce prin creşterea germenilor de fază solidă, formaţi fie din lichid (grupări de atomi), fie din impurităţi sau asperităţile recipientului în care se află lichidul. In cursul solidificării, atât cât subzistă două faze, una lichidă şi alta solidă, temperatura rămâne constantă. Căldura evacuată în timpul solidificării se numeşte căldură latentă de solidificare. O astfel de reacţie se numeşte exotermă.
Preview document
Conținut arhivă zip
- Stiinta Materialelor
- 10 Uzarea.doc
- 12 Studiul diagramelor de echilibru binare.DOC
- 14 Sticla.doc
- 5 Arhitectura spatiala a cristalelor.doc