Extras din notiță
1. Stări de agregare: Criterii de clasificare, abordare fenomenologică și statistică, caracteristici principale ale stării gazoase.
a. clasificare inițială atribuie substanțelor patru stări de agregare: solidă, lichidă, gazoasă și plasmă (materie stelară).
b. clasificare recentă evidențiază existența unor stări de agregare cu proprietăți noi sau intermediare, cum sunt stările de: cvasicristal, coloid și cristal lichid.
ABORDAREA STĂRILOR DE AGREGARE
a) din punct de vedere fenomenologic - se urmăresc doar proprietățile fizico-chimice accesibile măsurării directe, pentru a stabili relațiile existente între proprietăți, fără a ține seama de structura substanțelor.
b) din punct de vedere statistic - substanțele sunt formate din molecule, atomi, ioni care se mișcă și interacționează, iar proprietățile substanțelor se deduc din structura lor internă și din mișcarea și interacțiunea particulelor.
Principalele caracteristici
- mișcarea foarte intensă a moleculelor care determină o variație continuă a distanțelor intermoleculare
- difuzia foarte mare, cu tendința de a ocupa întreg volumul accesibil (gazele iau forma și volumul vasului în care se găsesc)
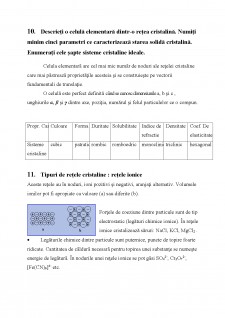
- variația mare a volumului cu presiunea și temperatura
- densitatea extrem de mică
- compresibilitatea ridicată
- gazele nu prezintă senzație la pipăit, au miros, pot fi incolore sau colorate
2. Legea Boyle - Mariotte
Definiție: La temperatură constantă, produsul presiunii și volumului unui gaz este constant.
(p1 - Vm1)T = cst = (p2 - Vm2) T=cst = (pn - Vm n ) T=cst = constant
3. Legea Gay - Lussac
Definiție: La presiune constantă, volumul unei cantități (1 mol) de gaz variază cu temperatura.
(Vm1 / T1)p = cst = (Vm2 / T2)p = cst =( Vm n /Tn)p = cst = constant
4. Legea lui Charles
Definiție: La volum constant, presiunea unei anumite cantități de gaz variază cu temperatura.
(p1/T1)Vm = cst = (p2/T2)Vm = cst = (pn /Tn)Vm = cst = constant
5. Legea lui Avogadro.
Definiție: Volume egale de gaze diferite, măsurate în aceleași condiții de presiune și temperatură, conțin același număr de particule (molecule) NA = 6,023 - 1023.
Preview document
Conținut arhivă zip
- Chimie fizica si coloidala.docx