Extras din proiect
Generalitati
Titanul face parte din subgrupa a patra a sistemului lui Mendeleev impreuna cu thoriul , hafniul si zirconiul, avand numarul de ordine 22 si o greutata atomica de 47,90. Desi este unul din cele mai raspandite elemente in scoarta terestra , mult timp a fost putin studiat, considerandu-se ca este un metal dur si casant si ca nu poate fi utilizat in tenica decat in calitate de dezoxidant.
A fost gasit in 1788 sub forma de bioxid si s-a extras sub forma unei pulberi in 1825 impurificata cu nitrura,iar pentru a obtine un metal de puritate corespunzatoare a trebuit sa treaca 100 de ani pana in 1925.
Literatura de specialitate a inceput sa se ocupe excesiv de mult de titan si aliajele sale abia din anul 1940, cand sunt comuniocate rezultatele obtinute la prelucrarea titanului maleabil ,extras prin descompunerea iodurii.Ulterior, s-a raspandit pe scara industriala metoda reduceri magneziotermice a tetraclorurii in atmosfera neutral sau in vid ,realizandu-se buretele de titatn care aliat cu alte metale si elaborate in cuptoare elecrtice cu vid cu electrozi consumabili a dat posibilitatea realizari aliajelor acestui metal[1].
Titanul este unul dintre principali componenti ai scoartei panantului adica in procent de 30 %.datorita dificultatilor procurari acestuia din minereuri a fost considerat un metal rar.
Culoarea tiatnului este alba argintie ,prezinta rezistenta la rupere intre 500 si 880 MPa, are temperature de topire de 1668˚ Csi temperature de fierbere de 3027˚ C, greutatea este specifica titanului 4,5 * 10 la 3 kg pe m la a 3 ,alunigirea este cuprinsa intre 4 si 28 %si duritatea de 180-260 HB.
La incalzire titanul se dilate de 2,5 ori mai putin decat aluminiul,iar rezistivitatea sa electrica este de 5 ori mai mare decat cea a fierului si de 20 de ori decat cea a aluminiului.
Titanul prezinta doua stari alotropice.Tiα stabil pana la 882˚ C si Tiβ stabil de la aceasta temperature pana la temperature de topire.Titanul prezinta o transformare similara celei martensitice fiind tratat termic datorita transformari alotropice. Prin calire la temperature superioare temperaturii de transformare alotropica se obtine o structura fina aciculara asemanatoare cu martensita, iar dupa revenire inalta la temperature imediat sub punctual alotropic structura se globulizeaza.
Influenţa elementelor de aliere asupra proprietăţilor titanului
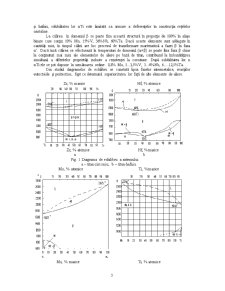
Zirconul şi hafniul – metale asemănătoare cu titanul – formează serii continue de soluţii solide cu ambele modificaţii alotropice, aşa cum se constată din diagramele de echilibru prezentate în figura 1, a, b. La călire, în aliajele bogate în titan din sistemul Ti-Zr, Ti-Hf, în domeniul de temperatură corespunzător fazei βTi, se produce transformarea martensică a fazei β în faza α’ ca şi la titanul pur. Numai la călirea aliajelor care conţin peste 20% Zr se poate fixa o oarecare cantitate de fază β. Aceste două elemente de aliere sunt folosite, deoarece măresc refractaritatea şi rezistenţa le fluaj a metalului. În afară de aceasta, ziconiul în aliajele Ti-Al conduce la îmbunătăţirea plasticităţii la fel ca elementele β stabilizatoare.
Mobibdenul, vanadiul, niobiul, tantalul sau reniul formează cu titanul sisteme de aliaje binare cu diagrame de stare aproape de zirconiu (fig 1.2, a, b, c, d), întru-cât ele fac parte din grupa a 5-a a sistemului lui Mendeleev, iar diamentrele atomilor lor diferă de cel al titanului cu mai puţin de 10 .15%, având reţea cristalină izomofă cu faza β. Spre deosebire de ziconiu şi hafniu, solubilitatea lor αTi este limitată ca urmare a deferenţelor în construcţia reţelelor cristaline.
La călirea în domeniul β se paote fixa această structură în proporţie de 100% în aliaje binare care conţin 10% Mo, 15%V, 36%Nb, 60%Ta. Dacă aceste elemente sunt adăugate în cantităţi mici, în timpul călirii are loc procesul de transformare martensitică a fazei β în faza α’. Dacă însă călirea se efectuează la temperaturi de domeniul (α+β) se poate fixa faza β chiar la conţinuturi mai mici ale elementelor de aliere pe bază de titan, contribuind la îmbunătăţirea simultană a diferitelor proprietăţi inclusiv a rezistenţei la coroziune. După solubilitatea lor n αTi ele se pot dispune în următoarea ordine: 0,8% Mo, 1 .3,5%V, 3 .4%Nb, 6 .12,5%Ta.
Din studiul diagramelor de echilibru se constată lipsa fazelor intermetalice, reacţiilor eutectoide şi peritectice, fapt ce determină superioritatea lor faţă de alte elemente de aliere.
Zr, % masice Hf, % atomice
Zr, % atomice Hf, %masice
a b
Fig. 1 Diagrama de echilibru a sistemului:
a – titan-zirconiu; b – titan-hafniu
Mo, % atomice Ti, %masice
Mo, % masice Ti, % atomice
a c
V, %masice Ta, % atomice
V, % atomice Ta, % masice
b d
Fig. 1.2 Diagrama de echilibru a sistemelor:
a – titan-olibden; b – titan-vanadiu;
c – titan-niobiu; d – titan-tantal
Cromul fiind izomorf cu βTi formeaza seria continua de solutii solide (fig. 1.3). Soluibilitatea lui αTi este mica (sub 0.5%), iar faza sufera o transformare eutectoida cu separarea fazei α si acompusului intermetalic TiCr2.
Preview document
Conținut arhivă zip
- Titanul si Aliajele Sale.doc