Extras din proiect
Fierul
Fierul este un element chimic metalic, notat cu simbolul Fe. Numărul său atomic este 26, iar masa atomică este 56. Fierul se află în grupa a 8-a şi perioada 4, fiind clasificat ca un metal tranziţional.
Fierul a fost cunoscut din cele mai vechi timpuri. Astăzi, dezvoltarea tehnicii moderne fiind strâns legată de folosirea fierului şi a aliajelor sale, se tinde spre o continuă perfecţionare a procedeelor de elaborare a fontelor şi a oţelurilor.
Răspândire în natură
Fierul este metalul greu cel mai răspândit în natură, alcătuind 4,7% din litosferă; în ordinea abundenţei, este al patrulea element din scoarţa pământului. Deşi poate exista şi în stare nativă, cantităţile cele mai însemnate de fier se cunosc sub formă de combinaţii. Minereuri de fier importante sunt: hematitul, un oxid de fier(III), Fe2O3, de culoare roşie, cu structură fibroasă, oligistul, un oxid de fier(III), Fe2O3, de culoare roşie, însă cristalizat; când oxidul de fier(III) este amestecat cu argilă se numeşte ocru roşu; limonitul este un oxihidroxid de fier(III), FeO(OH), care, amestecat cu argilă, formează ocrul galben; magnetitul, oxidul de fier(II)-fier(III), Fe3O4, se prezintă sub formă de octaedre negre strălucitoare; sideroza este un carbonat de fier(II), FeCO3, cristalizat în romboedre cenuşii-brune, iar pirita este o sulfură de fier, FeS2.
Cantităţi mari de fier se găsesc şi sub formă de silicaţi.
Minereurile de fier sunt extrem de răspândite în mai toate părţile globului.
Cele mai mari zăcăminte de fier la noi în ţară sunt la Ghelar, Teliuc şi la poalele munţilor Poiana Ruscăi din judeţul Hunedoara.
Mai există fier şi de natură meteoritică, el fiind component principal al meteoriţilor.(Aceştia sunt, de obicei, aliaje de fier cu 5-20% nichel.)
Compuşi ai fierului se mai găsesc încă în diferite ape minerale, ape de râuri, chiar în apa mărilor, cum şi în unele celule vegetale. Şi pentru corpul omenesc fierul are un rol important: este componentul necesar al hemoglobinei.
Obţinere
Există mai mulde metode pentru obţinerea fierului. În practică, alegerea uneia sau alteia dintre aceste metode se face după proprietăţile (în special puritatea) urmărite la fierul obţinut.
a. Reducerea oxizilor. Pentru obţinerea fierului pur reducerea se face cu hidrogen. În acest caz oxizii se prepară prin descompunerea unor combinaţii (oxalat, carbonat) purificate în prealabil. Reducerea oxizilor cu cărbune stă la baza procedeului industrial pentru fabricarea diverselor varietăţi tehnice de fier. Produsul obţinut prin această metodă nu este fier pur, ci aliaje de carbon şi alte câteva elemente.
b. Disocierea termică a combinaţiilor. Unele combinaţii ale fierului, de exemplu formiatul sau iodura feroasă, se descompun termic, punând în libertate metalul. Aplicaţie tehnică are disocierea pentacarbonilului de fier, Fe(CO)5, prin care se obţine fier de înaltă puritate, fin granulat, folosit în industria electrotehnică şi în metalurgia pulberilor.
c. Electroliza în soluţie apoasă a sărurilor feroase (FeCl2, FeSO4) dă de asemenea fier pur.
Mult mai importantă este, din punct de vedere economic, obţinerea fierului tehnic, aliaje de fier cu o cantitate mică de carbon în diferite proporţii: fonta şi oţelul.
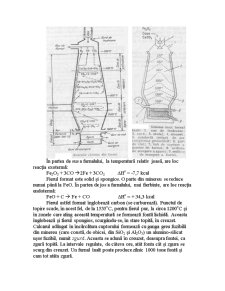
Metalurgia fierului (siderurgia). Acest procedeul industrial, aplicat pe scară largă, se bazează pe reducerea oxizilor de fier cu cărbune, în furnale înalte de dimensiuni mari, căptuşite cu cărămizi reflectare.
Preview document
Conținut arhivă zip
- Fierul.doc