Cuprins
- 1. Legi experimentale ale gazelor.
- 2. Transformarea izotermă.
- 3. Transformarea izobară.
- 4. Transformarea izocoră.
- 5. Principiul I al termodinamicii.
- 6. Principiul al II-lea al termodinamicii.
- 7. "Stările de agregare"(referat)
Extras din proiect
1.Legi experimentale ale gazelor
In unele cazuri, fluidele pot fi, considerate incompresibile,ceea ce pentru lichidele si gazele aflate la presiuni relativ mari, este in mare masura adevarat.Totusi,atunci cand apar schimburi de energie sub forma de caldura, fluidele, dar si corpurile solide, sufera variatii de volum, modificandu-se totodata presiunea exercitata asupra corpurilor cu care sistemul vine in contact.
Gazele sunt fluide cu densitati de circa o mie de ori mai mici decat ale lichidelor, si în mod normal, sunt foarte ușor compresibile.Caracterizarea stării de echilibru a unui gaz,închis într-o incintă, presupune precizarea presiunii și volumului ocupat de acesta la o anumită temperatură.
Dacă sistemul gazos efectuează schimburi de căldură cu mediul in care se află, constatăm modificări ale parametrilor care-i caracterizează starea.
2.Transformarea izotermă.
Definiție: Numim "transformare izotermă" acea transformare in cadrul căreia temperatura este constantă pe toată durata procesului.
Legea transformării izoterme a fost descoperită experimental în 1662 de către irlandezul Robert Boyle, cronologic, prima lege a gazelor care a fost descoperită.
T=cts.
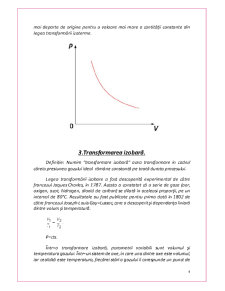
Într−o transformare izotermă, parametrii variabili sunt presiunea şi volumul gazului. Într−un sistem de axe, în care una dintre axe este presiunea, iar cealaltă este volumul, fiecărei stări a gazului îi corespunde un punct de coordonate (p, V), numite coordonate Clapeyron.
În coordonate p−V, reprezentarea grafică a unei transformări izoterme a gazului ideal este un arc de hiperbolă, simetrică faţă de prima bisectoare a sistemului de coordonate. Arcul de hiperbolă intersectează prima bisectoare mai departe de origine pentru o valoare mai mare a cantităţii constante din legea transformării izoterme.
3.Transformarea izobară.
Definiție: Numim "transformare izobară" acea transformare in cadrul căreia presiunea gazului ideal rămâne constantă pe toată durata procesului.
Legea transformării izobare a fost descoperită experimental de către francezul Jaques Charles, în 1787. Acesta a constatat că o serie de gaze (aer, oxigen, azot, hidrogen, dioxid de carbon) se dilată în aceleasi proporţii, pe un interval de 80°C. Rezultatele au fost publicate pentru prima dată în 1802 de către francezul Joseph Louis Gay−Lussac, care a descoperit şi dependenţa liniară dintre volum şi temperatură.
P=cts.
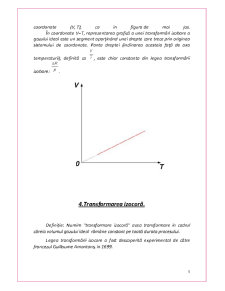
Într−o transformare izobară, parametrii variabili sunt volumul şi temperatura gazului. Într−un sistem de axe, în care una dintre axe este volumul, iar cealaltă este temperatura, fiecărei stări a gazului îi corespunde un punct de coordonate (V, T), ca în figura de mai jos.
În coordonate V−T, reprezentarea grafică a unei transformări izobare a gazului ideal este un segment aparţinând unei drepte care trece prin originea sistemului de coordonate. Panta dreptei (înclinarea acesteia faţă de axa temperaturii), definită ca , este chiar constanta din legea transformării izobare: .
Preview document
Conținut arhivă zip
- Portofoliu la Fizica.doc