Cuprins
- Introducere 3
- Oxidarea electrochimică – Mecanism 3
- Electrozi optimi oxidări electrochimice 4
- Cataliza în procesul de oxidare electrochimică 5
- Oxidarea electrochimică a etilenglicolului 6
- Celula electrolitică 6
- Mecanismul oxidării etilenglicolului 7
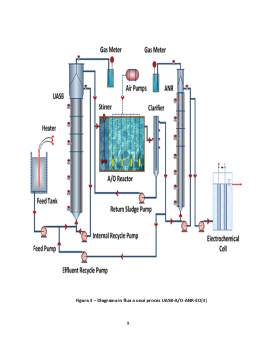
- Oxidarea electrochimcă – proces industrială 8
- Concluzii 10
- Bibliografie 11
Extras din referat
Industria chimică consumă o mare cantiate de apă pentru diferite procese,care conduc la cantităţi însemnate de apă reziduală.Apele reziduale sunt o combinaţie complexă de diferiţi compuşi organici si anorganici,dintre care unii pot fii sau deveni toxici sau pot fii foarte greu de îndepărtat. Mare majoritate a apelor sunt purficate cu ajutorul tratamentelor aerobice sau anaerobice fie prin coagulare chimică.Insă,aceste tehnici nu sunt suficiente pentru a înlătura toţi compuşi dăunători din apa reziduală iar pe lângă această limitare mai rezultă o cantitate ridicată de nămol toxic. De aceea pentru a mai diminua aceste probleme,s-au cuplat diferite tehnici de purificare a apei pentru a obţine rezultate căt mai bune iar tehnicile electrochimice cum ar fi oxidarea electrochimică,coagularea electrochimică sau floculaţia electrochimică au primit din ce în ce mai multă întrebuinţare pentru a elimina compuşi toxici din ape sau transformarea compuşilor organici într-o formă inofensivă pentru mediu sau pentru organismele vii.
Oxidarea electrochimică - MecanismApare prin oxidare directă de către radicalul hidroxil produs pe suprafaţa anodului sau prin oxidare indirectă cănd oxidanţi precum anionul clorură,hipoclorură,peroxid de hidrogen/ozon sunt produşi de către electrozi prin reacţiile următoare:
2Cl- → Cl2 + 2e-
Cl2 + H2O → HOCl + H+ + Cl-
HOCl → H+ + OCl-
H2O → OH + H + e−
2OH → H2O2
H2O2 → O2 + 2H+ + 2e−
O2 + O* → O3
Oxidarea indirectă apare atunci cănd speciile active de clor sunt generate din anioni anodici de clorură pentru a distruge poluanţi.În aşa numită oxidare electrochimică mediată,ionii metalici sunt oxidaţi la anod dintr-o stare stabilă la o stare reactivă adică valenţă ridicată care atacă direct poluanţi şi generează radicali liberi hidroxil care avansează starea de degradare a poluanţilor sau a compuşilor cu grad ridicat de toxicitate.[1]
În oxidarea electrochimică directă sau oxidarea anodică,oxidarea poluanţilor în cadrul celulei electrochimice apare la suprafaţa electrodului sau prin transfer direct de electroni la anod.De asemenea oxidanţii puternici numiţi specii reactive de oxigen se pot forma din apă la anod in timpul electrolizei,aceste specii sunt radicali liberi de hidroxil şi oxigenul molecular din structura oxizilor.Oxidarea anodică are anumite beneficii pe langă oxidarea indirectă cum ar fi lipsa nevoii de a adăuga alte substanţe adjuvante pentru a diminua poluarea şi o cantitate mai mică de substanţe toxice secundare rezultate.[1]
Electrozi optimi oxidări electrochimice
În cazul oxidări electrochimice a fost folosită o gamă largă de electrozi,dar pentru îmbunătăţi rezultatele s-a căutat materialul potrivit pentru oxidarea optimă a poluantului respectiv.Tradiţional anozii folosiţi pentru tratarea apei si a apelor poluate sunt confecţionaţi din plumb si oxizi de plumb,grafit sau diamant dopat cu bor. Plumbul si oxidul de plumb au fost utilizaţi ca material pentru anozi datorită stabilităţi lor,cost de realizare scăzut şi potenţial de evoluţie a oxigenului ridicat care favorizează evoluţia potenţialului de clor.Cu ajutorul electrozilor de plumb s-au realizat mineralizarea totală a 1,3,5-trimetoxibenzenului in mediu acid pe anod de Ta/PbO2, s-a descoperit de asemenea că toţi produşi de oxidare sunt in final oxidaţi la CO2 prin intermediari carboxilici.S-a descoperit şi faptul că activitatea electrocatalitică a electrodului de oxid de plumb depinde de electrolit,astfel că în prezenţă de acid sulfuric a apărut otrăvirea electrodului,deoarece un film aderent s-a format la suprafaţa acestuia.[1] Se folosesc electrozi de oxid de plumb dopaţi cu fier care au un potenţial de evoluţie a oxigenului mai mare decăt electrodului nedopat si o performanţă de oxidare electrochimică
Bibliografie
[1]H. Särkkä, A. Bhatnagar, and M. Sillanpää, “Recent developments of electro-oxidation in water treatment - A review,” J. Electroanal. Chem., vol. 754, pp. 46 - 56, 2015.
[2]K. Jardak, A. Dirany, P. Drogui, and M. A. El Khakani, “Statistical optimization of electrochemical oxidation of ethylene glycol using response surface methodology,” Process Saf. Environ. Prot., vol. 105, pp. 12 - 20, 2017.
[3]L. na Wu, D. wei Liang, Y. ying Xu, T. Liu, Y. zhen Peng, and J. Zhang, A robust and cost-effective integrated process for nitrogen and bio-refractory organics removal from landfill leachate via short-cut nitrification, anaerobic ammonium oxidation in tandem with electrochemical oxidation, vol. 212. 2016.
Preview document
Conținut arhivă zip
- Oxidarea electrochimica - Metoda de distrugere a substantelor organice toxice.docx