Cuprins
- I. INTRODUCERE 2
- II. CALCULUL ENTALPIEI DE REACŢIE 3
- III. APRECIERI ASUPRA STABILITĂŢII COMPUSILOR OBŢINUŢI ÎN COMPARAŢIE CU ALŢI COMPUŞI 4
- IV. CALCULUL ENTROPIEI DE REACŢIE 5
- V. APRECIERI CALITATIVE ASUPRA ENTROPIEI DE REACTIE 6
- VI. CALCULUL ENERGIEI LIBERE GIBBS G ÎN CONDIŢII STANDARD 6
- VII. APRECIERI ASUPRA SPONTANEITAŢII REACŢIEI ÎN SISTEM IZOLAT ŞI NEIZOLAT 7
- VIII. CALCULUL AFINITĂŢII DE REACŢIE ÎN CONDIŢII STANDARD 8
- IX. DETERMINAREA DEPENDENŢEI H =f(T ) 8
- X. DETERMINAREA DEPENDENŢEI S =f(T ) 10
- XI. DETERMINAREA DEPENDENŢEI G =f(T ) 11
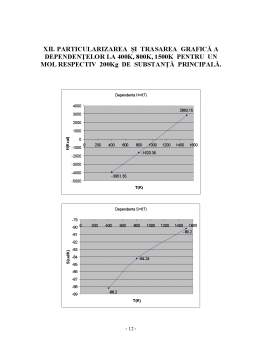
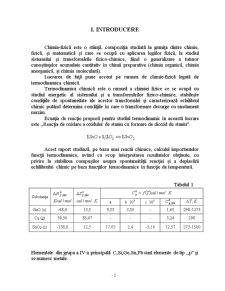
- XII. PARTICULARIZAREA ŞI TRASAREA GRAFICĂ A DEPENDENŢELOR LA 400K, 800K, 1500K PENTRU UN MOL RESPECTIV 200Kg DE SUBSTANŢĂ PRINCIPALĂ 12
- XIII. DETERMINAREA CONSTANTELOR DE ECHILIBRU k , k , k 15
- XIV. COMENTARII ASUPRA DEPLASĂRII ECHILIBRULUI CHIMIC 16
- XV. BIBLIOGRAFIE 16
Extras din referat
I. INTRODUCERE
Chimia-fizică este o stiinţă, compoziţia studiată la graniţa dintre chimie, fizică, şi matematică şi care se ocupă cu aplicarea legiilor fizicii, la studiul sistemului şi transformările fizico-chimice, fiind o generalizare a tuturor cunoştinţelor acumulate cantitativ în chimii preparative (chimia organică, chimia anorganică, şi chimia moleculară).
Lucrarea de faţă pune accent pe ramura de chimie-fizică legată de termodinamica chimică.
Termodinamica chimică este o ramură a chimiei fizice ce se ocupă cu studiul energetic al sistemului şi a transformărilor fizico-chimice, stabileşte condiţiile de spontaneitate ale acestor transformări şi caracterizează echilibrul chimic putând determina condiţiile în care o transformare decurge cu randament maxim.
Ecuaţia de reacţie propusă pentru studiul termodinamic în această lucrare este ,,Reacţia de oxidare a oxidului de staniu cu formare de dioxid de staniu”.
Acest raport studiază, pe baza unei reactii chimice, calculul importantelor funcţii termodinamice, având ca scop interpretarea rezultatelor obţinute, cu privire la stabilirea compuşilor asupra spontaneităţii reacţiei şi a deplasării echilibrului chimic pe baza funcţiilor termodinamice în funcţie de temperatură.
Tabelul 1
Substanţa
Elementele din grupa a IV-a principală C,Si,Ge,Sn,Pb sunt elemente de tip ,,p” şi se numesc metale.
Sn este un metal cunoscut din timpurile cele mai vechi Bronzul aliajul său cu Cu a dat numele unuia din primele epoci ale culturii omeneşti. În ţara noastră Sn mai este cunoscut şi sub denumirea de COSITERIT.
Sn se găseşte în natură mai ales sub formă de cositerit ( ) în rocile de granit alături de Cuarţ , minereuri de fier, Cu, Pb.
Proprietaţi fizice:
- este un metal alb cu strălucire argintie, frecat între degete lasă un miros neplăcut.
- dintre toate metalele de uz comun Sn are cea mai joasă temperatură de topire ( ).
Proprietăti chimice
- este stabil în aer.
- încălzit la se oxidează la suprafată la o temperatură mai înaltă se transformă în
Tabelul 2
Substanţa Ttopire Tfierbere
SnO (s) 1127
-1800 -1900
O2 (g) -218,4
-182,96
SnO2 (s) 1080
II. CALCULUL ENTALPIEI DE REACŢIE
Entalpia a fost introdusă pentru caracterizarea sistemelor şi proceselor fizico-chimice care se desfăsoară în condiţii de formare standard ce reprezintă cantitatea de căldură care însoţeşte entalpia unui mol de substanţă din elemente printr-o reacţie în care atât reactanţii cât şi produşii de reacţie se află în stări standard (1atm şi 25 ).
Entalpia este: - o marime energetică
- o marime extensivă: f (masa sistemului, numărul de moli)
Cele mai întâlnite entalpii de formare au valori negative.
Entalpiile de reactie pentru care condiţiile standard care însotesc reacţiile între corpuri compuse, se pot deduce din entalpiile de formare ale reactanţilor şi produşilor de reacţie care se calculează după următoarea formulă:
(1)
unde: =entalpia de reacţie
=entalpia de formare a produşilor
=entalpia de formare a reactanţilor
=coeficienţi stoechiometrici
În acest caz ecuaţia reacţiei este:
Preview document
Conținut arhivă zip
- Reactia de Oxidare a Oxidului de Staniu cu Formare de Dioxid de Staniu
- Parvu Radu.ppt
- PROIECT CHIMIE.doc