Cuprins
- Probleme generale 2
- 1.1. Evoluţia procedeului de electroliză a soluţiilor de clorură de sodiu 2
- 1.2. Electroliza soluţiilor de clorură de sodiu. Procese de electrod.
- Variante posibile 2
- 1.3.Clorul. Proprietăţi. Utilizări 3
- 1.3.1. Proprietăţile chimice ale clorului 3
- 1.3.2. Proprietăţile fizice ale clorului 5
- 1.3.3. Proprietăţile tehnologice 6
- 1.3.4. Domenii de utilizare 7
- 1.3.5. Producţia mondială de clor 7
- 2. Electroliza soluţiilor de clorură de sodiu prin procedeul cu membrană
- schimbătoare de ioni 8
- 2.1. Membrana schimbătoare de ioni (MSI) 8
- 2.2. Electrozi. Anozi. Catozi 9
- 2.3. Mecanismul procesului. Procese elementare. Procesul global 12
- 3. Prelucrarea fazei gazoase clor obţinută la electroliză 13
- 4. Procesul tehnologic de obţinere a clorului 14
- Bibliografie 16
Extras din referat
1. Probleme Generale
1.1. Evoluţia procedeului de electroliză a soluţiilor de clorură de sodiu
Clorul a fost cunoscut încă din secolul XVII. Până la apariţia procedeelor electrochimice acest produs s-a obţinut pe cale chimică, prin oxidarea acidului clorhidric.
În 1800 Cruickshank demonstrează posibilitatea descompunerii unei sări cu ajutorul curentului electric iar în anul 1986 Griesheim construieşte în Germania primul reactor electrochimic cu diafragmă destinat electrolizei soluţiilor de clorură de sodiu. Paralel cu dezvoltarea reactoarelor electrochimice cu diafragmă, apar şi se dezvoltă reactoarele cu catod de mercur, primul de acest fel apare în anul 1892 şi este opera lui Hamilton Zoung Castner. Apariţia în deceniul VIII al secolului XX a membranelor schimbătoare de ioni (NAFION®, Flemion®) a permis dezvoltarea celui de al treilea procedeu de electroliză a soliţiilor apoase de clorură de sodium – procedeul cu catod solid şi membrană schimbătoare de ioni. Acest procedeu, prin performanţele tehnologice, energetic şi ecologice superioare, tinde să elimine celelalte două procedee (electroliza cu catod solid şi diafragmă şi electroliza cu catod de mercur), ajungând în prezent să reprezinte un real concurent al procedeelor clasice.
România, ţară cu o tradiţie de peste 80 de ani în producţia clorului electrolitic, a introdus la sfârşitul anului 1996 primele instalaţii de electroliză cu membrană schimbătoare de ioni.
1.2. Electroliza soluţiilor de clorură de sodiu. Procese de electrod. Variante posibile.
Soluţia binară NaCl-H2O conţine în realitate ioni de clor şi de sodiu, oxoniul, hidroniul şi apa.
Într-o celulă de electroliză, încărcată cu soluţie de clorură de sodiu şi dotată cu electrozi de referinţă, la trecerea curentului electric au loc o serie de procese de electrod, numite procese anodice şi procese catodice.
La anod pot avea loc următoarele reacţii globale:
La catod, reacţiile globale posibile sunt:
În funcţie de pH-ul soluţiei, reacţiile (1.2) şi (1.3) pot fi scrise sub forma:
dacă pH < 7
dacă pH > 10
Electroliza soluţiilor apoase de clorură de sodiu se poate realiza în patru variante şi anume:
• electroliza cu catod solid şi clopot separator;
• electroliza cu catod solid şi diafragmă filtrantă;
• electroliza cu catod solid şi membrană schimbătoare de ioni;
• electroliza cu catod de mercur/ catod lichid.
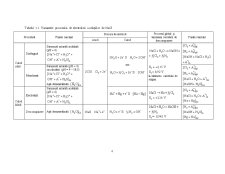
Variantele procesului de electroliză a soluţiilor de clorură de sodiu sunt prezentate în tabelul 1.1.
1.3.Clorul. Proprietăţi. Utilizări
Procesul de electroliză a saramurii cu membrană schimbătoare de ioni furnizează, conform celor prezentate în tabelul 1.1, patru faze produse de reacţie: clorul şi hidrogenul electrolitic, leşia de sodă caustică şi saramura epuizată. Cu excepţia saramurii, celelalte faze sunt prelucrate într-o succesiune de procese fizico-chimice, în vederea conferirii calităţii impuse de beneficiari. În urma acestor procese rezultă trei produse finite: clorul, hidrogenul şi soda caustică– alături de produsele secundare reprezentate prin soluţiile de hipoclorit de sodiu şi de acid sulfuric impur.
Clorul, rezultat în procesul de electroliză, numit clor electrolitic, reprezintă un produs intermediar. În funcţie de condiţiile locale, acesta este purificat, comprimat şi/sau lichefiat. Ca urmare, linia tehnologică poate furniza, clor electrolitic, clor purificat şi clor lichefiat.
Clorul poate fi caracterizat chimic, fizic şi tehnologic.
1.3.1. Proprietăţile chimice ale clorului
Ansamblul produs, fie el clor gazos sau clor lichid, conţine clor molecular drept component principal. Acesta este însoţit de o serie de impurităţi cum sunt: oxigen, azot, hidrogen, vapori de apă şi uneori de picături de saramură.
Clorul este un element deosebit de reactiv, urmând imediat după fluor. Ca urmare, se combină direct cu majoritatea elementelor, exceptând oxigenul, carbonul, azotul şi iridiul. Clorul gazos sau lichid este capabil să întreţină arderea, reducându-se uşor.
Preview document
Conținut arhivă zip
- Clorul in Procesul de Electroliza a Solutiilor de Clorura de Sodiu.docx