Extras din referat
Colagenul- definitie. Generalitati
Colagenul este principala proteină structurală din cele mai multe ţesuturi conjunctive moi, laxe, semirigide şi rigide (piele, oase, tendon, membrane bazale etc.), care asigură în principal integritate structurală ţesuturilor.
Datorită biocompatibilităţii şi biodegradabilităţii excelente, structurii bine definite, caracteristicilor biologice şi modului în care interacţionează cu organismul, colagenul reprezintă unul dintre cele mai utilizate biomateriale. Extras sub formă de soluţie apoasă sau gel, colagenul fibrilar tip I poate fi modelat în diferite forme: dispozitive medicale, implanturi artificiale, suporturi pentru cedarea medicamentelor şi schelete (scaffold) pentru regenerare tisulară, cu rol important în prezent în medicină.
2.Structura colagenului
Polimer natural, colagenul este constituit din 20 de aminoacizi, aranjaţi în secvenţe caracteristice, ce formează o structură conformaţională foarte complexă, organizată pe patru nivele, numite structuri primară, secundară, terţiară şi cuaternară.
Structura primară indică natura, numărul si secvenţa resturilor de α-aminoacizi din
lanţul α-polipeptidic, fără a considera aranjamentul spaţial. Compoziţia unui lanţ se exprimă
prin numărul de resturi dintr-un total de 100. Colagenii conţin 20 resturi diferite aranjate în
secvenţă regulată unică, lanţul fiind format din 1050-1100 resturi.
Lanţurile α-polipeptidice conţin cca 33% resturi de glicină (Gly), unul în fiecare a treia
poziţie, de prolină (Pro) – cca 9%, ale trei derivaţi ai aminoacizilor [4- si 5-hidroxiprolină
(Hyp) si hidroxilisină] situate în poziţii specifice faţă de Gly, de alanină – 11% si de
acizi glutamic si asparagic – 12%. Pro si Hyp constituie 22% din resturi, iar Gly, Pro si Hyp
cca 1/2 din totalul secvenţelor; nu conţine aminoacizi cu sulf si urme de aromatici.
Trăsătura distinctivă a colagenilor este aranjarea regulată a resturilor de aminoacizi în
lanţul a-polipeptidic: secvenţele Gly-Pro-Y si Gly-X-Hyp, X si Y fiind rest al oricărui alt
aminoacid. Cea mai frecventă este secvenţa Gly-Pro-Hyp. În lanţurile α ale colagenului tip I
matur sunt 338 asemenea secvenţe.
Aranjamentul spaţial local al atomilor dintr-un segment al lanţului principal, fără a ţine
seama de conformaţia lanţurilor sale laterale sau de relaţia cu alte segmente, este numită
structură secundară a acelui segment al lanţului polipeptidic.
În secvenţele Gly-Pro-Y si Gly-X-Hyp rotaţia în jurul legăturilor simple se combină cu
rigiditatea imprimată de resturile Pro si Hyp, ceea ce face ca lanţul să formeze spontan un
helix de tip poliprolină II (PPII), răsucit spre stânga, stabilizat de repulsia sterică a ciclurilor
pirolidinice din resturile Pro si Hyp. Conţinutul mare de asemenea resturi împiedică
formarea helixului α, întâlnit în cele mai multe proteine.
Helixul răsucit spre stânga este mult mai extins decât α, răsucit spre dreapta, motiv
pentru care nu se pot forma legături de hidrogen între grupele aceluiasi lanţ. Compoziţia
colagenului, neconvenabilă pentru formarea helixului α, este ideală pentru a forma un helix
triplu prin răsucirea spre dreapta, în jurul unei axe centrale comune, a trei helixuri răsucite
spre stânga, care constituie structura terţiară a colagenului.
Structura terţiară a unei molecule sau subunităţi de proteină reprezintă aranjamentul
spaţial al tuturor atomilor, fără a considera relaţia sa cu moleculele sau subunităţile vecine.
Conformaţia de helix triplu este stabilizată de legăturile de hidrogen ce se
stabilesc între cele trei lanţuri a-polipeptidice, decalate printr-un rest de aminoacid de cele de
Hyp, similar cu PPII.Pentru a se realiza împachetarea strânsă în jurul axei centrale
comune trebuie ca cel de al treilea rest să fie Gly, ceea ce duce la generarea secvenţelor triplet caracteristice lanţurilor a-polipeptidice ale colagenului.
Colagenul are o structura interna deschisa si contine un numar mare de situsuri de legare disponibile interactiei cu diferite substante biologic actuve: hormone, enzime, peptide.
Colagenii au fost definiti ca molecule ale matricei extracelulare ce contin secvente repetitive -Gly –X – Y , in care X si Y reprezinta aminoacizi care se pliaza intr-o structura unica triplu helicala.
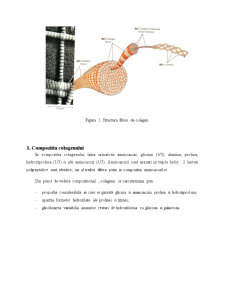
Din punct de vedere structural, colagenul este o scleroproteida, formata din macromolecule polipeptidice elicoidale, rasucite cate 3 impreuna si adunat in microfibrile, la randul lor inmanunchiate in fibrile, un numar mare din aceste formand fibra de colagen.
Figura 1. Structura fibrei de colagen
3. Compozitia colagenului
In compozitia colagenului intra urmatorii aminoacizi: glicina (1/3), alanina, prolina, hidroxiprolina (1/3) si alti aminoacizi (1/3). Aminoacizii sunt asezati in triplu helix : 2 lanturi polipeptidice sunt identice, iar al treilea difera putin in compozitia aminoacizilor.
Preview document
Conținut arhivă zip
- Colagenul.docx